Kekuatan Larutan Elektrolit

Hallo Otakers…. Artikel kali ini kita akan melanjutkan pembahasan mengenai Larutan Elektrolit dan Larutan Non Elektrolit. Nah sebelumnya kita sudah membahas apa itu komponen larutan dan daya hantar listrik pada bab Larutan Elektrolit dan Larutan Non Elektrolit. Pada artikel ini kita akan membahas Kekuatan Larutan Elektrolit, untuk lebih jelasnya kita bahas dibawah ini ya Otakers.
Apa Itu Larutan Elektrolit?
Larutan elektrolit adalah larutan yang dapat menghantarkan listrik, misalnya dengan ciri-ciri memberi gejala lampu menyala dan timbul gelembung gas pada batang karbon. Elektrolit umumnya berbentuk asam, garam atau basaLarutan elektrolit dibedakan menjadi dua, yaitu elektrolit kuat dan elektrolit lemah.
- Elektrolit Kuat yaitu Larutan elektrolit yang banyak menghasilkan ion-ion karena terurai sempurna. Larutan elektrolit kuat juga memiliki derajat ionisasi (α) = 1. Ciri-ciri larutan elektrolit kuat dapat dilihat dari nyala lampu dan menimbulkan gelembung gas pada batang karbon.
- Elektrolit Lemah yaitu Larutan elektrolit yang mengandung zat yang hanya sebagian kecil menjadi ion-ion ketika larut dalam air. Larutan elektrolit lemah memiliki derajat ionisasi (α) = 0 < α < 1. Ciri-ciri larutan elektrolit lemah dapat diketahui dari lampu tidak menyala tetapi menimbulkan gelembung gas.
Kekuatan Larutan Elektrolit
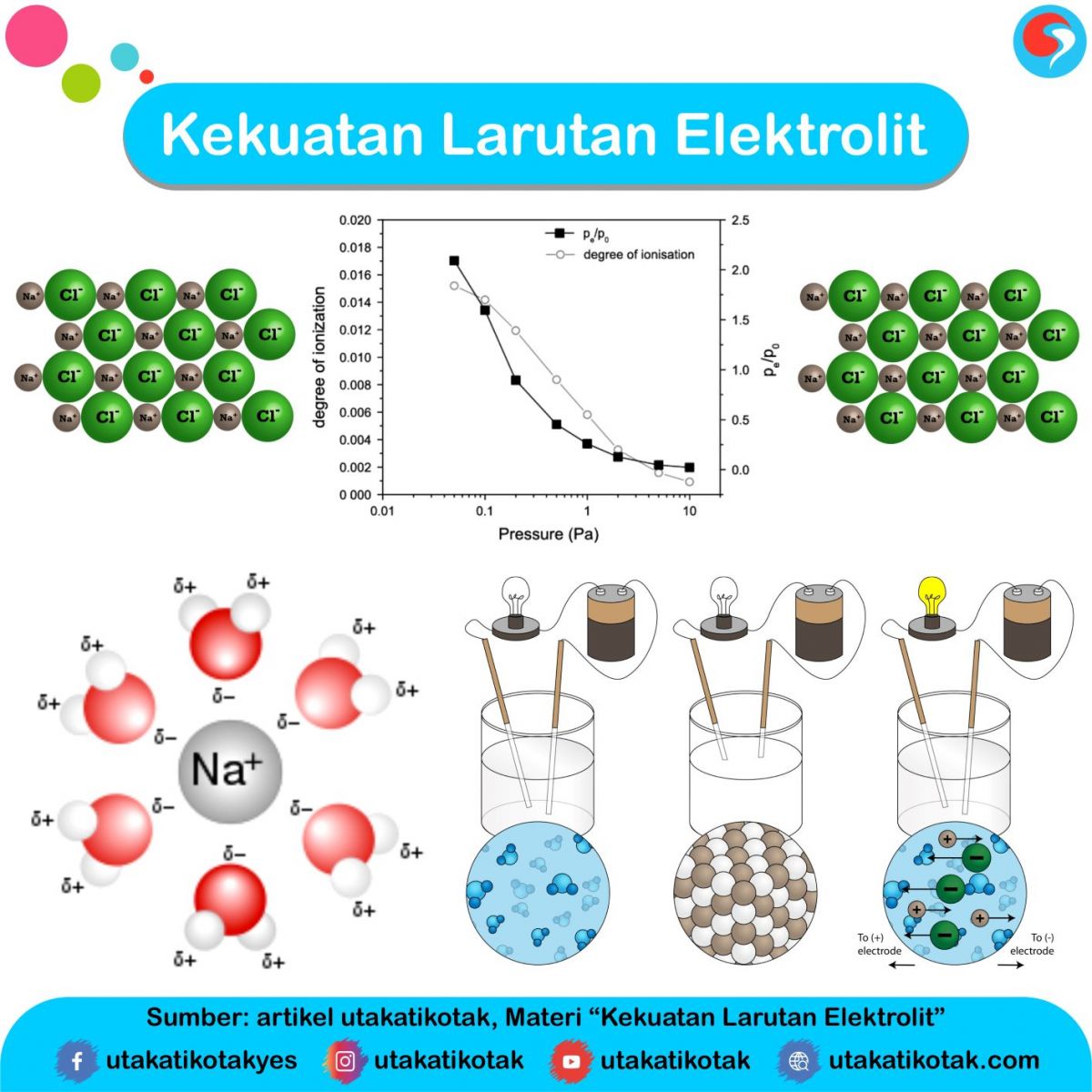
Dalam menentukan kuat tidaknya suatu larutan tergantung dari kemampuan ionisasi dari senyawa elektrolit yang diilarutkan dalam pelarut. Larutan elektrolit sebagaimana yang sudah kita jelaskan diatas dibagi menjadi 2 kelompok, elektrolit kuat dan elektrolit lemah. Terdapat tiga faktor yang dapat menentukan kekuatan larutan elektrolit, yaitu jumlah ion yang dihasilkan dari jenis larutan elektrolit, konsentrasi larutan dan derajat ionisasi.
- Jumlah Ion yang Dihasilkan dari Jenis Larutan Elektrolit
Jenis larutan elektrolit jika diurutkan berdasarkan jumlah ion yang dihasilkan adalah elektrolit kuat kemudian elektrolit lemah. Pada jenis elektrolit kuat senyawa terlarut akan menghasilkan banyak ion disuatu larutan, sedangkan untuk elektrolit lemah diketahui senyawa yang terlarut hanya menghasilkan ion dalam jumlah yang sedikit disuatu larutan. Misalnya pada suatu larutan mempunyai derajat ionisasi 0,00007, artinya untuk elektrolit lemah hanya mampu terurai sebanyak 0,007% dari total konsentrasinya, sedangkan elektrolit kuat hamper dapat menguraikan semuanya atau 100% dari konsentrasi terurai.
- Konsentrasi Larutan
Kekuatan larutan elektrolit ditentukan oleh konsentrasinya,semakin besar konsentrasi maka semakin besar kekuatannya. karena semakin banyak yang mengion. Misalnya pada larutan dengan konsentrasi rendah maka ion-ion akan mudah bergerak sehingga daya hantarnya menjadi semakin besar. Jika pada suatu larutan konsentrasinya tinggi atau pekat, maka pergerakan ion akan menjadi sulit sehingga daya hantarnya rendah.
Baca Juga :
Larutan Elektrolit dan Non Elektrolit (Komponen Larutan)
Daya Hantar Listrik Suatu Larutan
- Derajat Ionisasi
Nah, pembagian suatu zat tergolong elektrolit yang mana ditentukan berdasarkan nilai derajat ionisasi α. Apa yang dimaksud dengan derajat ionisasi? Derajat ionisasi adalah suatu perbandingan antara jumlah ion yang dihasilkan dengan jumal zat awalnya (mula-mula). Berikut ini rumus dari derajat ionisasi :

Pada larutan elektrolit kuat memiliki α = 1, dan pada elektrolit lemah memiliki 0<α<1. Derajat ionisasi sendiri memiliki rentang antara 0 sampai 1. Munculnya nilai α = 0 atau α =1 biasanya hanya untuk mempermudah penghitungan. Sehingga nilai derajat ionisasi akan berbanding lurus dengan kekuatan elektrolit. Untuk lebih jelasnya simak gambar dbawah ini ya.
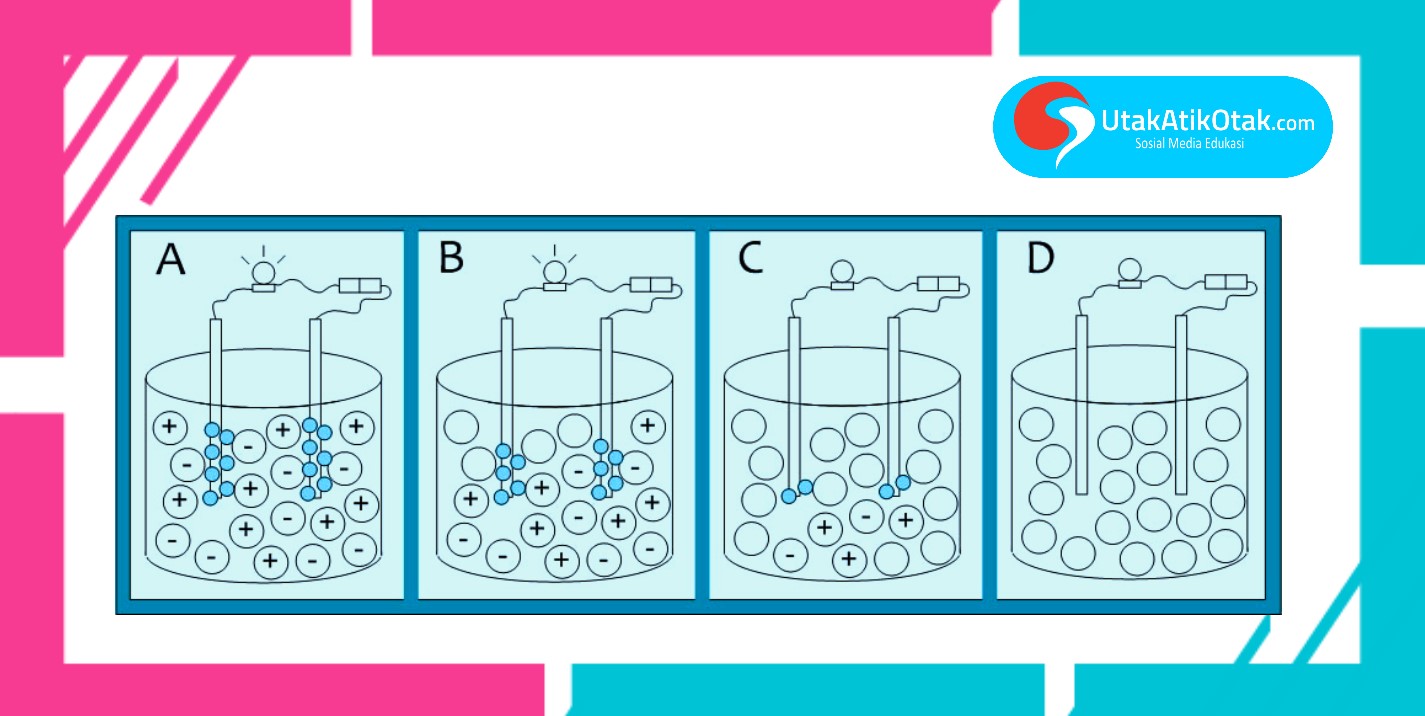
Pada gambar diatas dapat terlihat bahwa untuk Gambar A memiliki nilai derajat ionisasinya 1, dimana dapat diartikan bahwa gelembung yang dihasilkan dapat membuat lampu menyala karena semua larutannya membentuk ion.
Larutan Gambar B memiliki nilai derajat ionasisasinya mendekati nilai 1, jadi larutan Gambar B masih bisa menyalakan lampu karena Sebagian besar larutannya terionisasi.
Larutan Gambar C terlihat gelembung yang dihasilkan semakin sedikit sehingga pada Gambar C memiliki nilai derajat ionisasinya mendekati 0 sehingga lampu tidak dapat menyala, sedangakan untuk Gambar D terlihat tidak menghasilkan gelembung sehingga lampu tidak menyala karena nilai derajat ionisasinya 0.
Nah Otakers, itulah penjelasan singkat mengenai Kekuatan Larutan Elektrolit. Semoga bermanfaat. Salam dari Sabang sampai Merauke.
Artikel Terkait
- Suatu Larutan Jika Diuji dengan Alat Penguji Elektrolit Menunjukan Adanya Nyala Lampu yang Terang dan Timbulnya Gelembung Gas...
- Suatu Larutan Jika Diuji dengan Alat Penguji Elektrolit Menunjukan Adanya Nyala Lampu yang Terang dan Timbulnya Gelembung Gas
- Kristal NaCl Tidak Menghantarkan Listrik, Sedangkan Larutan NaCl Dapat Menghantarkan Lisrik
- Larutan Yang Dapat Menghantarkan Listrik Disebut? || Kuis Kimia || Kuis UAO
- Pengertian Sel Volta
- Apakah Air Garam Bisa Menghantarkan Arus Listrik?
- Senyawa Pembentuk Larutan Elektrolit
- Daya Hantar Listrik Suatu Larutan
- Larutan Elektrolit dan Non Elektrolit (Komponen Larutan)
- Hukum Faraday – Pengertian, Rumus, Bunyi dan Contoh Soal