Teori Asam Basa Lewis di Dalam ilmu Kimia
Sebelum membahas secara lebih detail tentang Teori Asam Basa Lewis yang diutarakan oleh Ahli Kimia Amerika Serikat, bernama Gilbert Newton Lewis (23 Oktober 1875 – 23 Maret 1946) maka ada baiknya bagi kalian para pembaca yang notabenya Pelajar, Mahasiswa ataupun Masyarakat Umum untuk mengetahui Pengertian Asam dan Basa itu sendiri.
Karena Pengertian Asam Menurut Ilmu Kimia memiliki artian sebuah Senyawa Kimia (Zat) yang dapat dilarutkan didalam Air dan akan menghasilkan Laruhan dengan pH yang lebih kecil dari 7 dan yang dapat memberikan Proton (ion H+) kepada Zat lain atau Senyawa Lain yang disebut dengan Basa. Sedangkan didalam Pengertian Basa menurut Ilmu Kimia adalah Zat (Senyawa Kimia) yang dapat beraksi dengan Asam, memberikan Senyawa yang disebut Garam dan Zat – Zat tersebut dapat menetralkan Asam.
Untuk Zat (Senyawa Kimia) Asam dan Basa ini saling berlawanan dan keduanya pun sering kita jumpai di kehidupan Manusia setiap harinya karena Zat (Senyawa Kimia) Asam ini ada didalam Cuka, Jeruk, Minuman Bersoda dan lain lain. Sedang Basa ada didalam Sabun, Bahan Pembuatan Pupuk dan lain lain. Oleh karena sangat baik sekali bagi kalian para Siswa Siswi untuk mengetahui secara lebih dalam tentang Zat (Senyawa Kimia) Asam dan Basa ini karena selain sering dijumpai di Kehidupan sehari – hari, Asam dan Basa tersebut pun sering muncul di Soal – Soal Ujian baik Ujian Sekolah atau Ujian Nasional di Mata Pelajaran Kimia.
Kemudian dikesempatan ini saya selaku penulis di Blog rumus rumus akan menjelaskan tentang salah satu Teori Asam dan Basa Menurut Lewis yang diutarakan di tahun 1932 silam oleh salah satu Ahli Kimia yang berasal dari Amerika Serikat, bernama Gilbert Newton Lewis karena sebelumnya saya telah menuliskan dan menjelaskan secara dalam tentang salah Teori Asam dan Basa yang lain yakni Teori Asam dan Basa Bronsted – Lowry dan tentunya telah ditulis dengan Sifat – Sifat Asam dan Basa nya.
Adapun perlu kalian tahu bahwa Teori Asam Basa dalam Ilmu Kimia telah terbagi menjadi 3 Teori Asam dan Basa yang antara lain Pertama Teori Asam Basa Arrhenius yang dikemukakan oleh Ahli Kimia Swedia bernama Svante August Arrhenius, Kedua Teori Asam Basa Bronsted Lowry yang dikemukakan oleh Dua Ahli Kimia yakni Jonannes Nicolaus Bronsted berasal dari Denmark dan Thomas Martin Lowry yang berasal dari Inggris serta yang ketiga ialah Teori Asam dan Basa Lewis yang dikemukakan oleh Ahli Kimia Asal Amerika Serikat yang bernama Gilbert Newton Lewis.
Bunyi Teori Asam Basa Lewis Secara Lengkap
Lalu didalam Teori Asam Basa menurut Lewis ini bahwa Asam merupakan suatu Senyawa Kimia (Zat) yang bisa menerima Pasangan Elektron dari Senyawa (Zat) lain atau bisa dikatakan Akseptor pasangan Elektron, sedangkan Basa Menurut Teori Asam Basa Lewis ialah suatu Senyawa Kimia (Zat) yang bisa memberikan pasangan Elektron kepada Senyawa yang lain atau bisa dikatakan sebagai Donor pasangan Elektron.
Teori Asam Basa Gilbert Newton Lewis ini merupakan sebuah Teori Asam Basa yang mengembangkan Teori Asam dan Basa Menurut Bronsted Lowry karena teori ini mempunyai keterbatasan dan kelemahan seperti saat menjelaskan reaksi – reaksi yang melibatkan senyawa tanpa proton (H+). Gilbert Newton Lewis berpendapat bahwa masalah Teori Asam-Basa harus diselesaikan dengan landasan Teori Struktur Atom, bukan hanya berdasarkan hasil percobaan (Penelitian) saja.
Contoh Teori Asam Basa Lewis Yang Ada
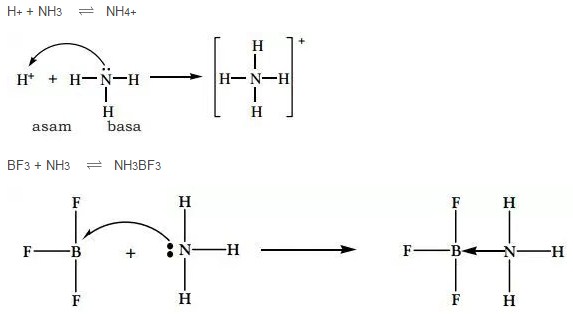
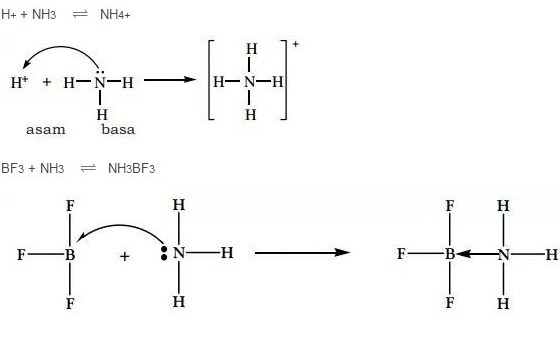
Contoh Teori Asam dan Basa Menurut Lewis pada Gambar diatas telah menunjukan bahwa Ion H+ (Proton) ialah Asam Lewis karena mampu menerima Pasangan Elektron, sedang NH3 merupakan Basa Lewis. Lalu pada reaksi antara BF3 dengan NH3 pada Gambar diatas yang merupakan Asam Lewis ialah BF3 karena bisa menerima sepasang Elektron dan teruntuk NH3 ialah Basa Lewis.
Untuk Kesimpulkan dari Perbedaan Teori Asam Basa Lewis dengan Bronsted Lowry adalah Teori Asam dan Basa Menurut Gilbert Newton Lewis lebih luas dan lengkap jika sepanjang yang dibahas didalamnya ialah Senyawa tanpa Proton, namun jika Reaksi Asam Basa yang melibatkan reaksi di Larutan dalam Air maka Teori Bronsted Lowrylah yang lebih mudah digunakan.
Artikel Terkait
- Introductions (Perkenalan)
- Sinonim akulturasi adalah kontak kabudayaan #sinonim #bahasa #akulturaasi #bahasaindonesia #antonim
- Pada Suatu Pertemuan, Hadir 10 Orang yang Saling Berjabat Tangan. Banyaknya Jabat Tangan yang Terjadi Adalah... Jawaban dan Pembahasan
- Suku Kelima Suatu Barisan Aritmatika Adalah 22, Sedangkan Kesembilan Adalah 42. Suku Kelima Belas Sama Dengan... Jawaban dan Pembahasan
- Mata Uang yang Sering Digunakan Sebagai Alat Pembayaran dan Kesatuan Hitung Dalam Transaksi Ekonomi dan Keuangan Internasional Disebut...
- Kingdom yang Tidak Memiliki Dinding Sel... Jawaban dan Pembahasan
- Organel Sel yang Berperan Untuk Mendetoksifikasi Racun Adalah... Jawaban dan Pembahasan
- Diketahui Harga 4 kg Jeruk, 1 kg Semangka, dan 2 kg Apel Adalah Rp 54.000,00. Harga 1 kg Jeruk, 2 kg Semangka, dan 2 kg Apel Adalah Rp 43.000,00. Sedangkan Harga 3 kg Jeruk, 1 kg Semangka, dan 1 kg Apel Adalah Rp 37.500,00. Berapakah Harga 1 kg Semangka?
- Nilai Rataan Hitung dari Data 4 10 7 x 10 6 11 Adalah 8 Nilai x Adalah ...
- Berikut ini Simbol yang Digunakan Dalam Operasi Hitung Pada Excel, Kecuali... Jawaban dan Pembahasan