Persamaan Umum Gas Ideal Lengkap dengan Contoh Soal

Gas ideal adalah gas yang mempunyai sifat-sifat yang sama pada kondisi yang sama. Keberadaan gas ideal biasanya ditemukan pada gas dengan tekanan rendah dan jauh dari titik cair karena dianggap mempunyai sifat-sifat gas ideal. Gas yang mempunyai sifat-sifat gas ideal akan memenuhi persamaan gas ideal.
Persamaan gas ideal dinyatakan dalam rumus umum gas ideal yang memuat hubungan antara tekanan (p), volume (V), jumlah mol (n), konstanta umum gas (R), dan suhu (K).
Gas ideal juga memiliki beberapa sifat yang menjadi pertanda mengenai sifat tersebut:
1. Memiliki partikel dalam jumlah banyak.
2. Tidak memiliki interaksi antarpartikel atau tidak ada gaya tarik menarik pada setiap partikelnya.
3. Apabila dilakukan perbandingan, kuran ruangan, ukuran partikel gas ideal bisa diabaikan.
4. Adanya tumbukan yang menimpa antara partikel gas dan dinding ruangan merupakan tumbukan lenting sempurna.
5. Setiap partikel gas memiliki persebaran secara merata di dalam satu buah ruangan.
6. Setiap partikel gas memiliki pergerakan secara serampang ke segala arah.
7. Hukum Newton berlaku dalam penerapan hukum tentang gerak.
8. Energi kinetik memiliki rata-rata molekul gas idela yang sebanding dengan suhu mutlaknya.
Persamaan Umum Gas Ideal
Besar tekanan gas dalam sebuah wadah dipengaruhi oleh suhu dan volume gas. Volume gas berbanding lurus dengan suhu mutlak gas pada tekanan tetap (isobarik) dan tekanan gas berbanding lurus dengan suhu mutlak gas. Sedangkan hubungan volume dan tekanan pada proses gas berbanding terbalik dengan suhu tetap.
Persamaan umum Gas Ideal dituliskan dengan rumus berikut.

Contoh Soal Gas ideal
Sebuah tangki bervolume 8.314 cm3 berisi gas oksigen (Mr = 32) pada suhu 47°C dan tekanan alat 25×105 Pa. Jika tekanan udara luar 1×105 Pa maka massa oksigen dalam tangki tersebut adalah …. (konstanta umum gas = 8,314 J/mol·K)
Pembahasan:
Berdasarkan keterangan yang diberikan pada soal dapat diperoleh informasi-informasi seperti berikut.
-
Volume gas: V = 8.314 cm3 = 8,314 ×10–3 m3
-
Massa relatif gas oksigen: Mr O2 = 32
-
Suhu: T = 47°C = 47° + 273° = 320 °K
-
Tekanan alat: P1 = 25×105 Pa
-
Tekanan udara luar: P2 = 1×105 Pa
-
Konstanta gas umum: R = 8,314 J/mol·K
Menghitung massa (m) gas oksigen dalam tangki:
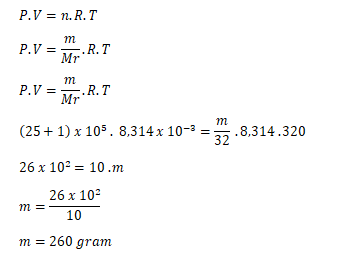
Jadi, massa oksigen dalam tangki tersebut adalah 260 gram.