Hukum Termodinamika 1 Dan 2 – Pengertian, Rumus, Contoh Soal
kali ini kita akan membahas materi tentang rumus hukum termodinamika 1 dan 2, kita akan jabarkan secara detail dan lengkap dari pengertian, bunyi hukum termodinamika, siklus, entropi, rumus dan contoh soal beserta pembahasannya.
Pengertian Termodinamika
Hukum Termodinamika
Termodinamika ialah bidang ilmu yang meliputi hubungan antara panas dan jenis energi lainnya. Termodinamika ditemukan dan diteliti awal abad 18. Pada saat itu, terkait dengan dan mendapat perhatian karena penggunaan mesin uap. Termodinamika dapat dipecah menjadi dua hukum.
Hukum I Termodinamika
Hukum I Termodinamika menyatakan bahwa :
“Jumlah kalor pada suatu sistem ialah sama dengan perubahan energi di dalam sistem tersebut ditambah dengan usaha yang dilakukan oleh sistem.”
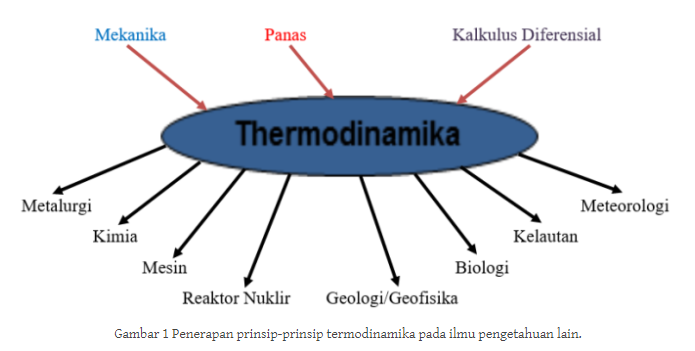
Hubungan antar kalor dan lingkungan dalam hukum I Termodinamika seperti yang ditunjukkan pada gambar 1.
Energi dalam sistem merupakan jumlah total semua energi molekul yang ada di dalam sistem.
Apabila sistem melakukan usaha atau sistem mendapatkan kalor dari lingkungan, maka energi dalam sistem akan naik. Sebaliknya jika energi dalam sistem akan berkurang jika sistem melakukan usaha terhadap lingkungan atau sistem memberi kalor pada lingkungan.
Dengan demikian dapat kita disimpulkan bahwa perubahan energi dalam pada sistem tertutup ialah selisih kalor yang diterima dengan usaha yang dilakukan sistem.
Rumus Hukum I Termodinamika
Dari bunyi hukum I Termodinamika, maka rumus hukum I Termodinamika dapat dituliskan sebagai berikut ini :
Q = ∆U + W ataupun ∆U = Q – W
Di mana :
∆U = Perubahan energi dalam sistem (J)
Q = Kalor yang diterima ataupun dilepas sistem (J)
W = Usaha (J)
Nonton Video Kita Juga Ya
Termodinamika (Part 1) || Hukum 1 Termodinamika Lengkap dengan Contoh Soal
Perjanjian pada hukum I Termodinamika
Rumus hukum I Termodinamika dipakai dengan perjanjian sebagai berikut ini :
1. Usaha (W) bernilai positif (+) jika sistem melakukan suatu usaha
2. Usaha (W) bernilai negatif (-) jika sistem menerima suatu usaha
3. Q bernilai negatif jika sistem melepaskan kalor
4. Q bernilai positif jika sistem menerima suatu kalor
Pengertian Siklus
Siklus merupakan serangkaian proses yang dimulai dari suatu keadaan awal dan berakhir pada keadaan yang sama dengan keadaan awalnya. Agardapat melakukan usaha terus-menerus, suatu sistem harus bekerja dalam satu siklus. Ada 2 macam siklus, yakni siklus reversibel (siklus yang dapat balik) dan irreversibel (siklus yang tidak dapat balik).
Siklus Carnot
Siklus Carnot
Gambar diatas ialah gambar siklus mesin pemanas carnot. terdapat empat proses dalam siklus Carnot, yakni :
- pemuaian dengan cara isotermik (a-b)
- pemuaian dengan cara adiabatik (b-c)
- pemampatan dengan cara isotermik (c-d)
- pemampatan dengan cara adiabatik (d-a)
Mesin Kalor Carnot
Proses dalam mesin kalor Carnot, perhatikanlah gambar siklus carnot diatas. Siklus dapat dijelaskan sebagai berikut ini :
- Siklus a-b
Gas menyerap kalor Qt pada temperatur Tv Suhu sistem sama dengan suhu reservoir panas sehingga dapat disebut proses isotermik. Gas memuai dan melakukan suatu usaha pada pengisap. Oleh karena energi dalam tetap maka usaha yang dikerjakan pada sistem sama dengan kalor yang diserap. - Siklus b-c
Beban pengisap dikurangi sehingga menyebabkan gas memuai menurut proses adiabatik. Terjadinya pengurangan energi dalam dan suhu sistem menurun sampai sama dengan suhu pada reservoir dingin Tr - Siklus c-d
Gas mengalami penyusutan dengan cara isotermik dengan membuang kalor Qrpada reservoir dingin pada temperatur 7) sehingga usaha negatif (usaha dilakukan pada sistem). - Siklus d-1
Beban pengisap ditambahkan sehingga gas menyusut menurut proses adiabatik. Terjadinya penambahan energi dalam dan suhu naik sampai sama dengan suhu pada reservoir panasT. Energi dalam suatu gas kembali seperti pada awal siklus.
Usaha pada mesin pemanas Carnot :
W = Qt – Qy
Karakteristik mesin kalor carnot dinyatakan dengan efisiensi mesin (η) yakni perbandingan antara usaha yang dilakukan dengan kalor yang diserap. Secara matematis ditulis sebagai berikut ini.
Sistematis
Efisiensi suatu mesin kalor jenis apapun selalu lebih kecil dari efisiensi mesin ideal atau mesin Carnot.
Berdasarkan hukum I Termodinamika berlaku:
Berdasarkan Hukum I Termodinamika
Keterangan:
η : efisiensi mesin
Tr : temperatur pada reservoir rendah
Tt ; temperatur pada reservoir tinggi
Qr : kalor yang dibuang pada reservoir rendah
Qt : kalor yang diserap pada reservoir tinggi
Mesin Pendingin Carnot
Contoh dari mesin pendingin Carnot antaralain mesin pendingin ruangan dan lemari es. Siklus mesin pendingin Carnot adalah kebalikan siklus mesin kalor Carnot karena siklusnya ialah reversibel (dapat balik).
Usaha pada mesin pendingin Carnot dapat dituliskan sebagai berikut ini :
W= Qt — Qr
Karakteristik pada mesin pendingin dinyatakan dengan koefisien performansi atau koefisien kinerja dengan simbol Kd. Koefisien kinerja didefinisikan sebagai perbandingan usaha antara kalor yang dipindahkan dengan usaha yang dilakukan sistem.
Mesin Pemanas Carnot
Dari Gambar sebelumnya diatas dapat dijelaskan bahwa kalor yang diambil dipindahkan ke dalam ruangan.
Karakteristik mesin pemanas dinyatakan dengan koefisien kerja dengan simbol Kp . Secara matematis dapat dituliskan sebagai berikut ini :
Secara Sistematis
Hukum II Termodinamika
Hukum II Termodinamika menyatakan bahwa :
” Kalor mengalir secara alami dari benda yang panas kebenda yang dingin; kalor tidak akan mengalir secara spontan dari benda dingin ke benda panas tan pa dilakukan usaha”.
Penjelasan hukum II Termodinamika ialah sebagai berikut ini :
- Tidaklah mungkin membuat mesin yang bekerja dalam satu siklus, menerima kalor dari satu reservoir dan mengubah kalor seluruhnya menjadi usaha.
- Tidaklah mungkin membuat mesin yang bekerja dalam satu siklus dengan mengambil kalor dari reservoir yang mempunyai suhu rendah dan memberikannya ke reservoir suhu tinggi tanpa usaha dari luar.
- Mesin yang bekerja di antara reservoir suhu Tt dan reservoir suhu Tt(Tt > Tr), mempunyai efisiensi maksimum.
Pengertian Entropi
Entropi dapat kita diartikan sebagai ukuran ketidakteraturan. Dalam sistem tertutup peningkatan entropi disertai oleh penurunan jumlah energi yang tersedia. Semakin tinggi entropi, semakin tinggi pula ketakteraturannya.
- Entropi pada Proses Temperatur Konstan
Jika suatu sistem pada suhu mutlak T mengalami proses reversibel dengan menyerap sejumlah kalor Q maka kenaikan entropi ∆S dapat dituliskan sebagai berikut ini :∆S = S2 – S1 = Q/T
Keterangan :
∆S : perubahan entropi (J/K)
S1 : entropi mula-mula (J/K)
S2 : entropi akhir (J/K)
- Entropi pada Proses Temperatur Berubah
Pada proses yang mengalami perubahan temperatur, entropi dituliskan sebagai berikut ini :
Entropi Pada Temperatur
Keterangan :
∆S : perubahan entropi (J/K)
S1 : entropi mula-mula (J/K)
S2 : entropi akhir (J/K)
c : kalor jenis (J/kg K)
m : massa (kg)
T1 : suhu mula-mula (K)
T2 : suhu akhir (K)
Contoh Soal Beserta Pembahasannya
1. Suatu mesin mempunyai suhu reservoir tinggi 400°C dan suhu reservoir rendah 70°C. Hitunglah efisiensi pada mesin tersebut!
Penyelesaian :
Diketahui :
Tt = 400°C atau 673 k
Tr = 70°C atau 343 K
Ditanyakan : η
Jawab:
Jawaban 1
Maka, efisiensi mesin sebesar 49%
2. Suatu sistem menyerap kalor sebesar 60 kJ pada suhu 27°C. Berapakah perubahan entropi sistem tersebut?
Penyelesaian :
Diketahui:
Q = 60 kJ atau 60. 000J
T = 27°C atau 300 K
Ditanyakan :
Jawab:
Jawaban 2
Maka, besar perubahan entropi adalah 200J/K
Inilah tadi pembahasan lengkap mengenai materi tentang rumus termodinamika, Semoga bermanfaat…
Artikel Terkait
- Sejumlah gas ideal dipanaskan hingga suhunya 2 kali semula pada tekanan tetap dengan mengambil kalor dari sumber panas sebesar 300 j untuk melakukan kerja sebesar 250 j. selama siklus terjadi besarnya energi dalam yang dikerjakan oleh gas sebesar
- Suatu mesin Carnot, jika reservoir panasnya bersuhu 400 K akan mempunyai efisiensi 40%. Jika reservoir panasnya bersuhu 640 K, efisiensinya menjadi …. %.
- Mesin Carnot bekerja pada suhu tinggi 600 K mempunyai efisiensi 40%. Agar efisiensi mesin naik menjadi 75% dengan suhu reservoir rendah tetap, maka reservoir suhu tinggi harus dinaikkan menjadi ... ?
- Contoh Soal Termodinamika (Fisika SMA) - Go Royong With Agiv
- Hukum 3 Termodinamika (Fisika SMA) - Go Royong With Agiv
- Pengertian Termodinamika
- Contoh Soal dan Pembahasan Teori Kinetik Gas
- Teori Kinetik Gas dan Sifatnya
- Ringkasan Materi Suhu dan Kalor
- Ringkasan Materi Suhu dan Kalor







